Isobar prosess
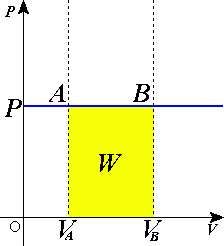
Ein isobar prosesss er ein termodynamisk prosess der trykket er konstant, . Varmen som blir overført til systemet gjer eit arbeid, men endrar òg den indre energien til systemet:
ifølgje termodynamikken si første lov der W er arbeidet gjort av systemet, U er indre energi, og Q er varme. Trykk-volum arbeid (av systemet) er definert som:
men sidan trykket er konstant betyr dette at
- .
Ved å bruke den ideelle gasslova får vi
når mengda av gass er konstant (til dømes ved at det ikkje skjer faseendringar). Sidan det generelt er slik at
så kan ein sette dei to siste likningane inn i den første likninga:
- .
Storleiken i parentes er den spesifikke varmen ved konstant trykk:
og visst gassen likninga gjeld for er einatomisk er og .
Entalpi
Ein isokor prosess er skildra som . Ein kan få ei liknande likning for isobare prosessar. Om ein set inn den andre likninga i den første får ein
Storleiken U + P V er ein tilstandsfunksjon kalla entalpi, og blir uttrykt som H. Derfor kan ein skildre ein isobar prosess som
- .